FAG i praksis
Analyser ved kjent hiv-infeksjon
Analyser ved kjent hiv-infeksjon.pdf(130 KB)
Hiv angriper immunforsvaret og gir en kronisk virusinfeksjon som ubehandlet fører til alvorlig immunsvikt. Viruset smitter seksuelt, via blod og blodprodukter, samt fra mor til barn i forbindelse med svangerskap, fødsel og amming. Den første tiden etter smitte kan viruset påvises i høye konsentrasjoner i plasma. Ubehandlet vil som regel viruskonsentrasjonen i blod avta i løpet av de første fire til seks måneder (1,2). Mengden hiv-RNA vil deretter stabiliseres på et nivå som varierer fra person til person og vil så igjen begynne å stige etter hvert som pasienten utvikler en økende grad av immunsvikt.
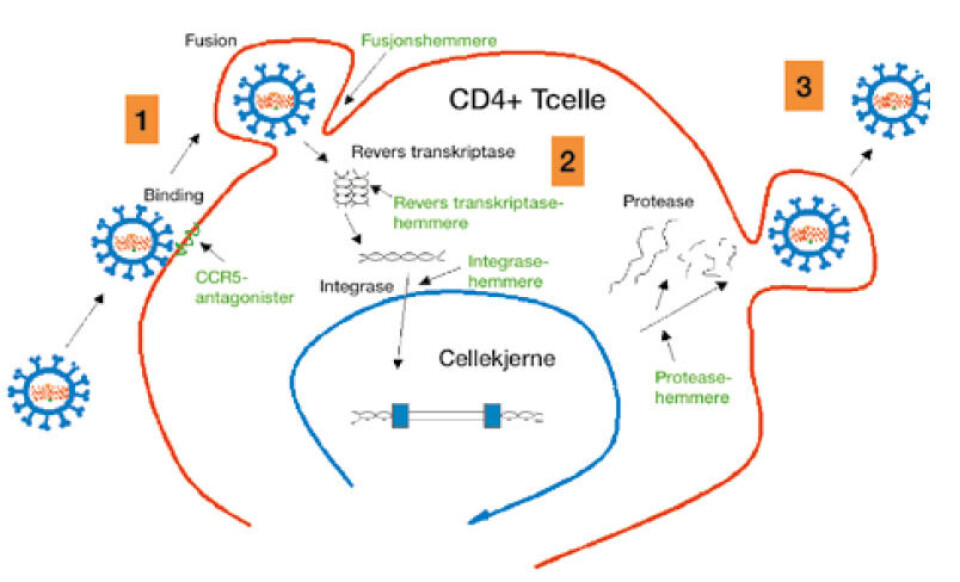
Innføring av antiviral behandling ved hiv-infeksjon har ført til en dramatisk reduksjon i hiv-relatert sykelighet og dødelighet. Det finnes i dag en rekke ulike medikamenter som benyttes i behandlingen av hiv-infeksjon, og disse er rettet mot ulike faser av hivs livssyklus (figur 1). Strategien for antiretroviral behandling er å benytte en kombinasjon av flere medikamenter fra ulike medikamentklasser med ulike angrepspunkter for å unngå utvikling av resistens.
Behandlingen eliminerer ikke virus fullstendig, men kan effektivt redusere produksjonen av nye viruspartikler. Ved effektiv antiviral behandling vil hiv-RNA-mengden ofte være så lav at den ikke detekteres. Et lite stopp i medisineringen vil derimot raskt kunne gi økende hiv-RNA-verdier i blodet og øke risikoen for utvikling av resistens.
Medikamentell resistens er dessverre en mulig begrensende faktor for langvarig effektiv behandling. Pasienter med erkjent kronisk hiv-infeksjon følges opp regelmessig ved infeksjonsmedisinske poliklinikker med klinisk undersøkelse og ulike blodprøver, som oftest hver tredje eller sjette måned. For disse pasientene benyttes ulike virologiske analyser som hjelpemiddel til å følge sykdomsutviklingen og monitorere behandlingen.
Virusmengden i blodet sier noe om sykdomsprogresjon, og benyttes til å følge effekten av antiviral behandling. Ved økende virusnivå under pågående behandling, kan man undersøke virusets følsomhet for ulike antivirale medikamenter. Slik undersøkelse av resistens er sammen med klinisk oppfølging et viktig redskap ved valg av behandling og ved eventuelt bytte av medikamentregime. Resistenstesting skal også utføres hos pasienter med nydiagnostisert hiv-infeksjon som ledd i nasjonal overvåking av mulig smitte med resistent virus.
Hiv-1 RNA kvantitering
Mengden fritt sirkulerende hiv-RNA i blod hos pasienter med kjent hiv-infeksjon, sier noe om virusets evne til å reprodusere seg selv i kroppen. Målet med antiviral behandling, er å svekke virusets evne til reproduksjon slik at mengden hiv-RNA i plasma stabiliserer seg på et nivå under 20 kopier per milliliter. Ønsket effekt av behandlingen er at mengden hiv-RNA skal ligge under 500 kopier per milliliter etter 12 uker og under 50 kopier per milliliter etter 24 uker (1). For å måle mengde fritt sirkulerende hiv-RNA i blod og følge effekten av behandlingen, utføres hiv-RNA kvantitering.
På Ullevål utføres kvantitering av hiv-1 RNA ved hjelp av en nukleinsyreamplifikasjonstest fra Roche: COBAS AmpliPrep/COBAS TaqMan HIV-1 test, som har en deteksjonsgrense på 20 kopier per milliliter (3). Et kjent antall hiv-1 kvantiteringsstandard-RNA molekyler (QS-RNA) tilsettes hver prøve og følger hele analyseprosessen parallelt med prøven. Viruspartiklene lyseres, og frigjort hiv-1 RNA og QS-RNA bindes til magnetiske glasspartikler. Etter vask for å fjerne ubundne substanser, blir den ferdig preparerte prøven med frigjort hiv-1 RNA og QS-RNA tilsatt en amplifikasjonsblanding og overført til analyse med COBAS TaqMan.
Dette er en realtids PCR-maskin som utfører revers transkripsjon, PCR med deteksjon og kvantitativ beregning. For å beregne mengde hiv-1 RNA for hver enkelt prøve, sammenliknes deteksjonsresultatet for prøven (CT) med deteksjonsresultatet til kvantiteringsstandarden.
Det er viktig å være klar over testens begrensninger. COBAS Ampliprep/COBAS TaqMan HIV-1 test, versjon 2.0, har en variasjonskoeffisient på opp til 41 prosent (3). Dette innebærer at påvist mengde hiv-1 RNA for en prøve kan variere nokså betydelig dersom samme prøve analyseres flere ganger. I oppfølgingen av pasienter med hiv-1 infeksjon, må denne variasjonen tas med i vurderingen av behandlingseffekt. En prøve med litt høyere kopitall enn forventet, er ikke nødvendigvis ensbetydende med dårlig behandlingseffekt. Flere kontrollprøver over tid vil avdekke om pasienten har oppnådd god antiviral respons eller ikke.
I tillegg til testens presisjon, er det viktig å være klar over viktigheten av riktige preanalytiske betingelser. Fordi RNA lett kan nedbrytes, vil stabiliteten til hiv-1 RNA i blod påvirkes av en rekke ulike faktorer. Rask og korrekt separering av plasma fra blodceller er trolig det viktigste, men også faktorer som prøvetakning, type antikoagulans og tid før nedfrysning eller analysering vil påvirke resultatet. Noen ganger må vi derfor avvise pasientprøven på grunn av feil prøvemateriale eller for gammelt materiale.
Anbefalt prøvemateriale er plasma med EDTA som antikoagulant. Det er ønskelig at det benyttes rør med gel. Ved sentrifugering vil gelen separere blodcellene fra plasma, noe som gjør at plasmaet er holdbart i 72 timer. Standard EDTA-rør (uten gel), må sentrifugeres og plasma må avpipetteres innen seks timer etter prøvetakning.
Sentrifugering av EDTA gelrør må utføres i henhold til gjeldende pakningsvedlegg for best mulig separasjon av blodceller og plasma.
En stor del av prøvene til hiv-1 RNA kvantitering blir tatt på EDTA gelrør, som oftest av typen Vacutainer PPT K2E (Becton-Dickinson) eller Vacuette K2E (Greiner Bio-One). Dersom disse rørene benyttes i prøvetakningen, er det viktig at rørene resentrifugeres etter ankomst til laboratoriet. Infiserte leukocytter kan lekke gjennom gelmembranen under transport. Disse cellene kan inneholde proviralt hiv-DNA som vil amplifiseres i PCR-analysen. Resentrifugering før avpipettering av plasma fjerner eventuelle leukocytter, og forhindrer dermed muligheten for falsk forhøyede kopitall (4,5).
Et stort antall prøver til hiv-1 RNA kvantitering mottas daglig, og prøver fra infeksjonsmedisinske poliklinikker utgjør hovedtyngden. De aller fleste prøvene som mottas er EDTA-plasma, men vi kan også analysere spinalvæske. Før analysering av spinalvæske er det viktig å sentrifugere vekk eventuelle blodceller. Dersom infiserte celler blir værende i spinalvæsken, vil proviralt hiv-DNA amplifiseres i tillegg til fritt sirkulerende hiv-1 RNA og gi falsk forhøyede kopitall. EDTA-plasma skal alltid tas samtidig med spinalvæsken for optimal sammenlikning av mengde hiv-1 RNA (ratio). EDTA-plasma og tilhørende spinalvæske bør helst analyseres i samme oppsett.
Kvalitativ hiv-2 RNA PCR
For kvalitativ påvisning av hiv-2 RNA, benyttes in-house konvensjonell nested RT-PCR. Det endelige PCR-produktet påvises til slutt med gelelektroforese. Testen benyttes på prøver fra pasienter med erkjent hiv-2 infeksjon, og prøvematerialet er EDTA-plasma.
Folkhälsomyndigheten i Sverige utfører kvantitering av hiv-2 RNA to ganger i året (mai og november). Vi anbefaler at prøver som skal til hiv-2 kvantitering først sendes til Ullevål for kvalitativ hiv-2 RNA PCR. Dersom vi påviser hiv-2 RNA, blir prøven videresendt til kvantitering. Er hiv-2 RNA ikke påvisbart med vår metode, er det ikke nødvendig å videresende prøven.
Genotypisk hiv-1 resistensbestemmelse
Mistanke om behandlingssvikt er den kliniske hovedindikasjonen for å utføre en genotypisk resistensundersøkelse. Økning i virusmengde under pågående behandling kan gi mistanke om at behandlingen ikke er effektiv. Selv om det kan være ulike forklaringer på en slik økning, er det ofte aktuelt å undersøke hvilke medikamenter pasientens virus er følsomt for. Vi kan da utføre en genotypisk resistensbestemmelse, der vi undersøker virusets følsomhet for de ulike proteasehemmere, revers transkriptasehemmere og integrasehemmere.
Før eventuell endring av behandlingsregimet kan man også gjøre en genotypisk undersøkelse av hiv co-reseptor tropisme dersom oppstart med CCR5-antagonister vurderes. Genområder som koder for de enzymene som medikamentene er rettet mot, blir amplifisert og sekvensert. Deretter leter man etter mutasjoner som man vet er assosiert med medikamentell resistens.
En annen viktig indikasjon for undersøkelsen er som ledd i nasjonal overvåking av smitte med resistente virus. Resistensbestemmelse av protease og revers transkriptase utføres på nydiagnostiserte så tidlig som mulig etter påvist hiv-infeksjon og før behandling startes. Vi sender anonymiserte sekvenser koblet til pasientenes meldenummer til Folkehelseinstituttet, som samler all genotypisk sekvensdata fra pasienter med nyoppdaget hiv-infeksjon i Meldingssystem for smittsomme infeksjonssykdommer (MSIS) og i Resistensovervåking av virus i Norge (RAVN) (6).
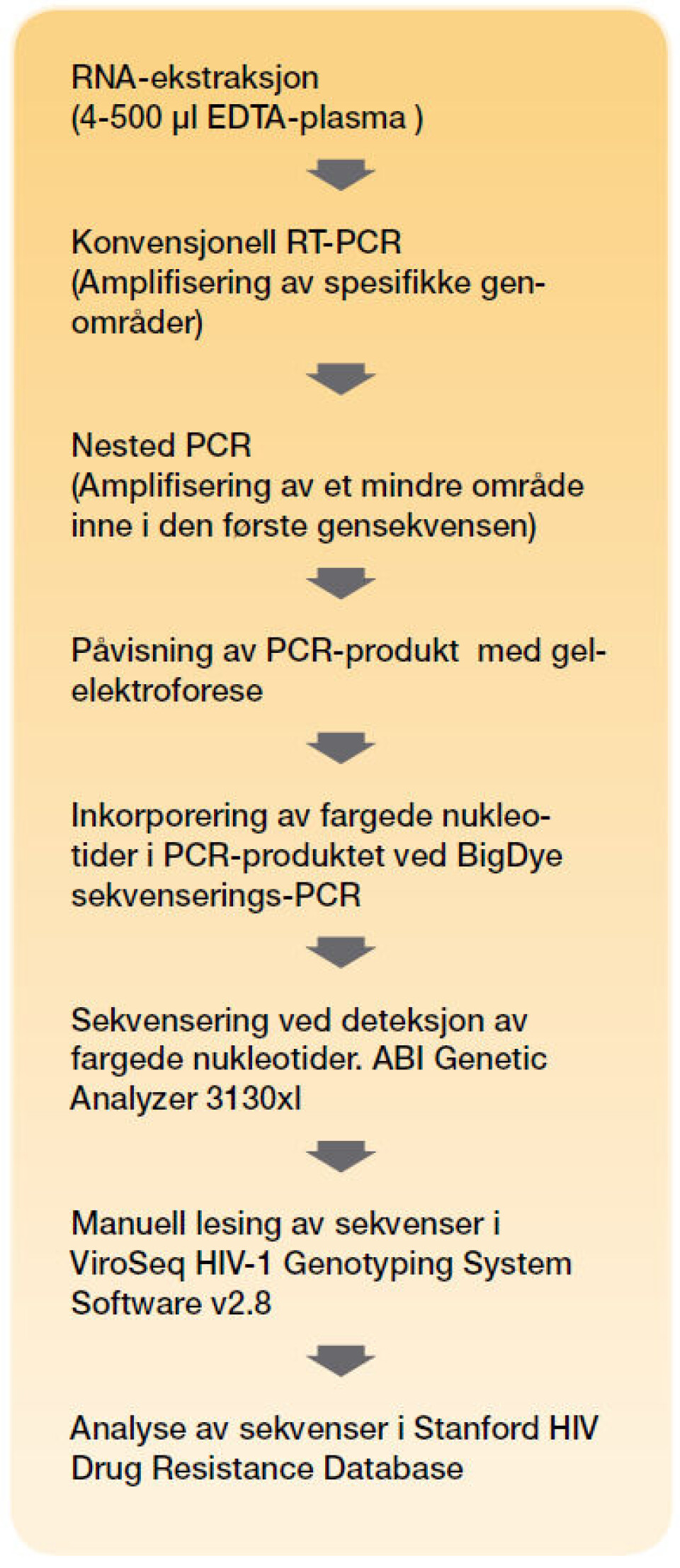
Genotypiske resistensundersøkelser utføres i EDTA-plasma, og de samme prøvene som skal til hiv-1 RNA kvantitering kan benyttes. For å utføre genotypisk hiv-1 resistensundersøkelse kreves et virusnivå på minimum 1000 kopier per milliliter plasma, men vi kan i noen tilfeller sekvensere prøver med lavere kopitall (ned til cirka 500 kopier per milliliter plasma). Ekstraksjon utføres manuelt eller automatisk. Rutinemessig benyttes 500 mikroliter plasma til manuell ekstraksjon og 400 mikroliter plasma til automatisk ekstraksjon. Manuell RNA-ekstraksjon øker fleksibiliteten og sensitiviteten siden vi kan benytte opp til én milliliter plasma som utgangsmateriale i prøver med lave kopitall. RNA amplifiseres med konvensjonell RT-PCR og deretter nested PCR (in-house) for å øke spesifisiteten. PCR-produktene påvises med gelelektroforese og fortynnes før BigDye sekvenserings-PCR (se figur 2).
Til undersøkelse av protease og revers transkriptase, benyttes et kommersielt kit fra Abbott til BigDye sekvenserings-PCR. Selve sekvenseringen gjøres i sekvensator ABI Genetic Analyzer 3130xl. Seks forskjellige primere (tre i hver retning) benyttes for å få sekvensert de aktuelle områdene for mutasjoner assosiert med resistens i proteasegenet og revers transkriptasegenet.
Til genotypisk hiv-1 resistensbestemmelse for integrasehemmere benyttes tilsvarende metode, men med in-house primere for amplifikasjon og sekvensering av genområdet som koder for integrase (7,8).
Sekvensene analyseres manuelt i ViroSeq HIV-1 Genotyping System Software v2.8, et program laget for hiv-1. Et annet web-basert program for automatisk lesing av sekvenser, Recall beta v2.9, kan også benyttes, men programmet er avhengig av god primerdekning i hele genområdet i begge retninger. Når sekvensene er nøye gjennomgått lagres gensekvenser som deretter lastes inn og analyseres i Stanford HIV Drug Resistance Database (figur 2).
Det finnes en database ved Stanford University som nå består av mer enn 90 000 hiv-sekvenser fra mer enn 80 000 isolater samlet fra Europa, Canada og USA og den oppdateres jevnlig. Gensekvensene blir behandlet i en tolkingsalgoritme for hiv-1 genotypisk resistens, og resulterer i en rapport som angir grad av resistens for protease-, revers transkriptase- og integrasehemmere. Endelig klinisk tolking av resultater blir gjort av erfarne overleger med spesialkompetanse innen hiv-resistens ved henholdsvis Infeksjonsmedisinsk avdeling og Mikrobiologisk avdeling, Ullevål.
Genotypisk hiv-1 resistensbestemmelse i Norge utføres kun på Mikrobiologisk avdeling ved OUS, Ullevål. Det skal benyttes egne rekvisisjoner. Det finnes en egen rekvisisjon for pasienter som står eller har stått på behandling der medikamentell behandling skal angis, og en annen for resistensovervåking hos nydiagnostiserte der MSIS meldenummer må oppgis.
Konklusjon
En stadig utvikling mot bedre medikamenter gir pasienter med hiv-infeksjon økt livskvalitet og forlenget levetid. Enklere medisinering og jevnlig oppfølging med kvantitering bidrar til bedret viruskontroll, noe som igjen kan redusere risikoen for utvikling av resistens.