Fag i praksis
Når forskning haster
Når nye og svært alvorlige bivirkninger av covid-19-vaksiner rapporteres, er det nødvendig at studier som kan belyse årsaker og insidens utføres og publiseres så raskt som mulig.
Av SVETLANA LUND, RENATHE HENRIKSEN GRØNLI, CHRISTIANNE SOLBØ, MARTHE PEDERSEN, TOM SOLLID, SIW LEIKNES ERNSTSEN, KJERSTI DAAE HORVEI, MARIE THERESE AHLÉN, HARALD STRAND
Når forskning haster.pdf(188 KB)
For å kunne stoppe spredning av SARS-Cov-2, viruset som forårsaker covid-19-sykdom, er store vaksinasjonsprogrammer satt i verk globalt. Flere ulike vaksiner er tilgjengelig, hvorav fire er godkjent i EU og Norge. Overvåkning av virkninger og bivirkninger følges opp også etter at vaksinene er godkjent. I midten av mars 2021 tok flere land pause i bruken av AstraZenecas covid-19-vaksine etter meldinger om tilfeller av tromboser etter vaksinering.
I første halvdel av mars ble fem helsearbeidere innlagt ved Rikshospitalet i Oslo med et svært alvorlig klinisk bilde, sju til ti dager etter at de hadde fått første dose av AstraZeneca-vaksinen. Tre av de fem pasientene døde. Hos disse pasientene ble det påvist svært høye nivåer av antistoffer mot platefaktor 4-polyanion-kompleks. Dette er antistoffer som også ses ved den alvorlige tilstanden heparinindusert trombocytopeni (HIT), samt den mer sjeldne autoimmun heparinindusert trombocytopeni (aHIT) (1, 2).
Godt samarbeid mellom fagfolk ved Oslo universitetssykehus (OUS) og Universitetssykehuset Nord-Norge (UNN) resulterte i en publikasjon i The New England Journal of Medicine, hvor disse fem pasientkasusene beskrives (3). Samtidig rapporterte også Greinacher et al. (4) tilsvarende funn hos vaksinerte i Tyskland. Den alvorlige bivirkningstilstanden betegnes nå som vaksineindusert immun trombotisk trombocytopeni (VITT). Det er også kommet flere rapporter om VITT fra andre fagmiljøer (5, 6).
Ved Nasjonal behandlingstjeneste for avansert trombocyttimmunologi ved Universitetssykehuset Nord-Norge har vi det fullstendige analyserepertoaret som er nødvendig for å påvise de blodplateaktiverende anti-PF4-antistoffene (7).
Studie med smalt tidsvindu
Tidligere er det rapportert at opptil sju prosent av normalbefolkningen kan ha anti-PF4-antistoffer uten at disse gir et klinisk bilde som ved HIT (8). Det er ikke tidligere beskrevet forekomst av anti-PF4-antistoffer etter covid-19-vaksinering. Vi ønsket derfor å undersøke om anti-PF4-antistoff og/eller trombocytopeni er til stede hos et større utvalg AstraZeneca-vaksinerte individer. Vi ønsket også å registrere bivirkninger hos disse.
Om lag 1500 helsearbeidere ved UNN var blitt vaksinert med AstraZenecas covid-19-vaksine i perioden fra februar til 11. mars, og vi mottok en rekke henvendelser fra UNN-ansatte som var bekymret for om de hadde dannet antistoffer mot platefaktor 4-komplekser, slik som rapportert hos VITT-pasientene. Tidsvinduet for å kunne gjennomføre en slik studie var imidlertid svært smalt. Dette fordi bruken av AstraZeneca-vaksinen nå var satt på pause og vi ønsket å samle inn prøver fra de vaksinerte i en sammenlignbar tidsperiode etter vaksinering som VITT-pasientene.
Vi ønsket også å se på utbredelsen av slike antistoffer i en uvaksinert kontrollgruppe som ikke tidligere hadde gjennomgått SARS-Cov-2-infeksjon. Denne kontrollgruppen bestod av blodgivere ved Blodbanken UNN Tromsø. Det var viktig å publisere slike data raskt dersom de skulle kunne inngå i beslutningsgrunnlaget vedrørende videre bruk av vaksinen.
Hva gjorde vi?
Sammenhengen mellom den alvorlige sykdomstilstanden VITT og AstraZeneca-vaksinen ble fastslått torsdag 18. mars, og i løpet av få dager ble det utarbeidet et prosjekt for å undersøke inntil 500 helsearbeidere etter deres første AstraZeneca vaksinedose, inkludert godkjenning fra Regional Etisk Komite (REK) og Personvernombud.
Etter helga ble AstraZeneca-vaksinerte ved UNN invitert til å delta i studien, og på et effektivt oppstartsmøte tidlig mandag morgen ble strategien lagt for hvordan laboratoriet best kunne gjennomføre den praktiske delen av studien. Fra UNN avga omtrent 430 studiedeltakere blodprøve, og med seks glass fra hver utgjorde dette over 2500 prøver som skulle håndteres. Prøvetakingen ble fordelt over tre påfølgende dager. I samme tidsperiode ble det også samlet inn to ekstra glass fra 110 friske blodgivere til kontrollgruppen. For at avdelingen skulle klare å gjennomføre et slikt omfattende prosjekt, ble åpningstiden ved prøvetakingsenheten utvidet og mange ansatte ved Laboratoriemedisin gjorde en ekstra innsats utover den ordinære driften for å utføre prøvetaking, prøvefordeling og biobanking. Køvakter passet på at smittevernreglene ble fulgt, samtidig som de holdt humøret i køa oppe og kontrollerte at samtykkeskjema var korrekt utfylt.
En betydelig preanalytisk arbeidsinnsats ble altså lagt ned før man i det hele tatt hadde startet å analysere innsamlet data. Samtidig med at vi samlet inn prøver ved UNN startet også Sykehuset Østfold tilsvarende prøveinnsamling. Totalt ble 502 deltakere inkludert i studien, 432 fra UNN og 70 fra Østfold. 10 deltakere ble seinere ekskludert på grunn av ufullstendig datasett (figur 1).
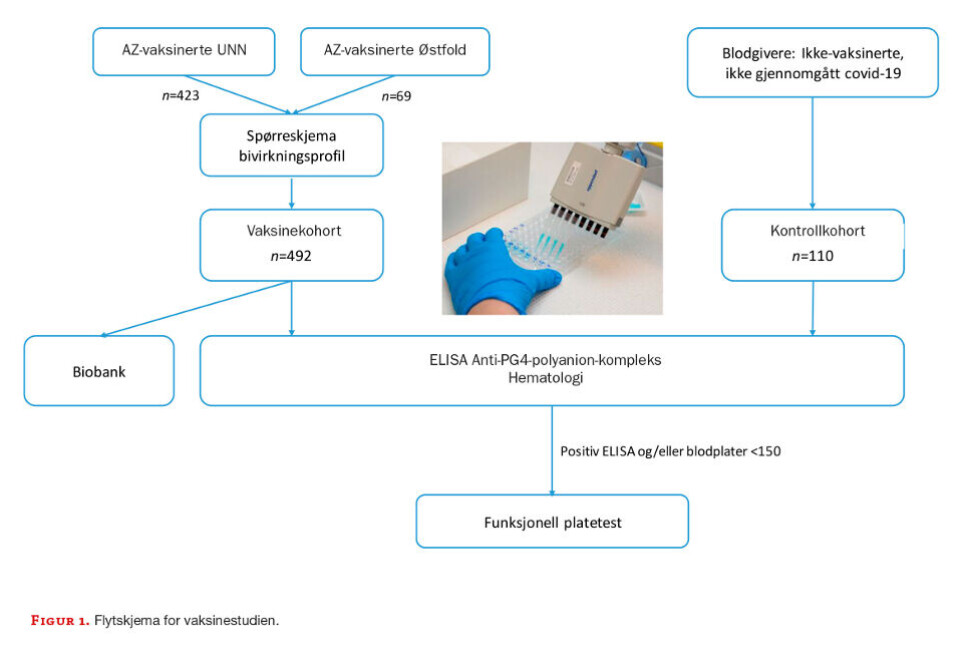
Etter prøvetaking ble prøvene fortløpende analysert for trombocytter og øvrige hematologiparametere med hematologianalysator. Forekomsten av antistoffer mot platefaktor 4-polyanion-kompleks ble undersøkt med ELISA-teknikk. Prøver som hadde antistoffmengde over referanseverdi ble analysert med en funksjonell HIMEA (Heparin Induced Multiplate Electrode Aggregation)-test som undersøker om anti-PF4-antistoff har evne til å aktivere og aggregere trombocytter. I denne testen inkuberes pasientens serum med blod fra blodgiver i parallelle tester med eller uten tilsatt heparin, i enten lav eller høy konsentrasjon (1).
Hva fant vi?
I denne studien fant vi antistoffer over referanseverdi hos seks av de 492 vaksinerte, hvorav ingen hadde reduserte trombocyttverdier eller positiv funksjonell HIMEA-test. Blant de vaksinerte hadde åtte studiedeltakere trombocytopeni (trombocytter <150*109/L), hvorav alle hadde verdier over 100*109/L. Ingen i kontrollgruppen av uvaksinerte blodgivere hadde positiv antistoff-test.
Våre funn tyder på at både naturlig forekomst og vaksineindusert forekomst av slike anti-PF4-antistoffer er sjelden. Resultatene fra vaksinestudien ble publisert i Journal of Thrombosis and Haemostasis ((JTH) 28. april. Artikkelen er fritt tilgjengelig (Open Access) hos JTH (9). Tilsvarende data er også nylig publisert fra forskergruppen i Greifswald, Tyskland (10).
Rask gjennomføring
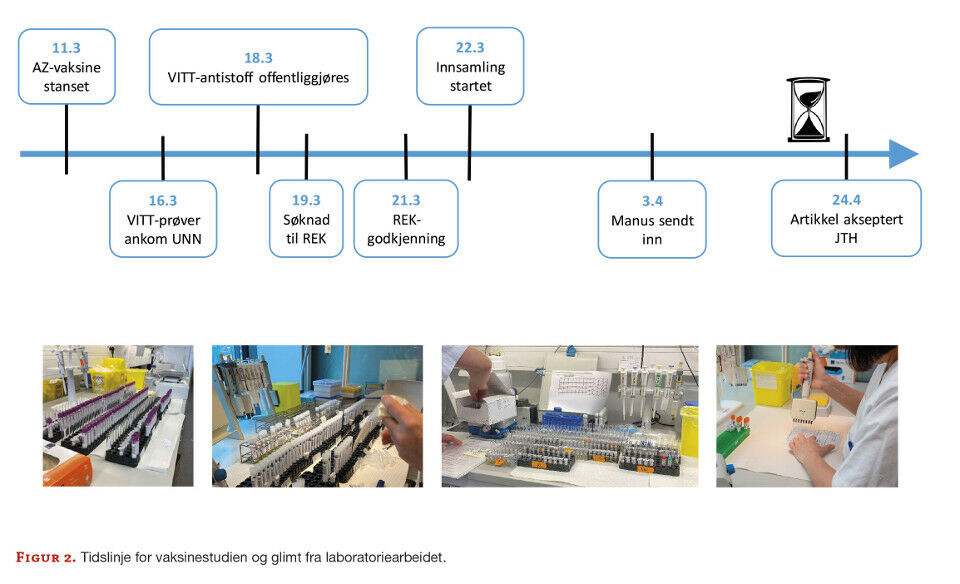
Forskningsstudier tar vanligvis måneder fra planlegging til gjennomføring. Ofte tar også analysering, artikkelskriving og publisering flere måneder, i noen tilfeller også år. Under alvorlige helsekriser som den pågående koronapandemien er det behov for at viktige kliniske funn og forskningsresultater raskt gjøres kjent. Det gikk kun tre uker fra vi tok fatt på arbeidet med å utrede de første meldte tilfellene av alvorlige bivirkninger etter AstraZeneca-vaksinen til resultatene var publisert i et internasjonalt tidsskrift. For vaksinestudien tok det seks uker fra REK-søknaden ble levert til hele vaksinestudien var gjennomført og publisert (figur 2). Dette viser at det er fullt mulig å både gjennomføre og publisere viktig forskning raskt.
Takk
Tusen takk til alle ansatte ved Laboratoriemedisin, UNN – og til Forskningsavdelingen og Senter for laboratoriemedisin, Sykehuset Østfold. Takk også til alle deltakerne i studien. Vaksinestudien har mottatt økonomisk støtte fra Helse Nord RHF.
Les også artikkelen "Lynrask forskning på UNN"
























