Neonatal alloimmun trombocytopeni
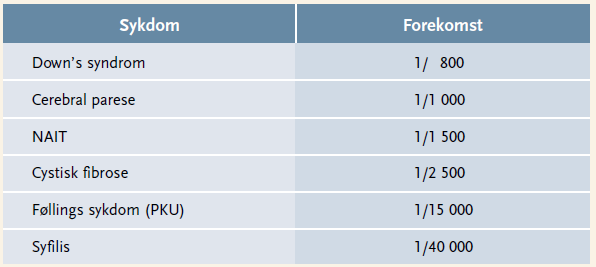
NAIT hos foster eller nyfødt er en sjelden, men alvorlig tilstand (1:1500, tabell 1) (1). Alloantistoffer til stede i mors sirkulasjon, som er rettet mot fosterets blodplater, vil kunne passere placentaen og binde seg til antigen uttrykt på fosterets blodplater og dermed føre til at blodplatene destrueres. NAIT defineres som alvorlig når barnets blodplatetall er < 50 x 109/L. Alvorlig NAIT behandles effektivt med transfusjon av forlikelige blodplater til den nyfødte. Transfusjoner med blodplater fra tilfeldige blodgivere er ikke like effektivt, men vil være den riktige behandlingen ved ukjent/nyoppdaget NAIT inntil forlikelig blodplatekonsentrat foreligger (2).
Flere humane blodplateantigener (HPA) spiller viktige roller ved ulike immunbetingede trombocytopenier. Antistoffer rettet mot HPA 1a forårsaker de fleste og de mest alvorlige tilfellene av NAIT (1). HPA 1 sitter på integrin β3 (GPIIIa), som sammen med integrin αIIb (GPIIb) danner blodplatenes fibrinogen reseptor. For hvert HPA system er en person enten homozygot for et av allelene (HPA 1aa eller HPA 1bb), eller heterozygot (HPA 1ab). Det mest vanlige allele har fått navnet a, mens det mindre vanlige allele har fått navnet b. Blant kaukasiere uttrykker 98 prosent HPA 1a allelet, og kun 2 prosent er HPA 1a negative (homozygote HPA 1bb). Forskjellen på integrin β3 som uttrykker HPA 1a eller 1b, er kun på én aminosyre.
De to prosentene som ikke uttrykker HPA 1a, kan risikere en immunisering dersom de eksponeres for paternelt HPA 1a uttrykt hos fosteret/barnet. Ti prosent av de gravide som er HPA 1a negative (HPA 1bb), danner antistoff mot barnets blodplater (anti-HPA 1a antistoff) og risikerer dermed å føde et barn med alvorlig NAIT (3). HLA DRB3*0101 har vist seg viktig i immuniseringen mot HPA 1a og ca 90 prosent av de immuniserte HPA 1bb kvinnene er HLA DRB3*0101 positive (3).
Nasjonalt referanselaboratorium for avansert blodplateimmunologi ved Universitetssykehuset Nord Norge (UNN), utreder immunologisk betingede blodplatesykdommer, og blodprøver fra hele landet sendes laboratoriet for analysering. Laboratoriet mottar blodprøver til utredning for NAIT når det uventet fødes et barn med blødninger eller når det tilfeldigvis oppdages trombocytopeni uten symptomer. NAIT kan gi akutte blødninger og gir symptomer som spontane hudblødninger like etter fødselen eller store hematomer etter injeksjoner, for eksempel etter vitamin K-injeksjon. Den mest alvorlige komplikasjonen i forbindelse med NAIT er blødninger i hjernen. Studier har vist at 13-26 prosent med alvorlig NAIT får hjerneskade på grunn av blødningskomplikasjoner (4-7). Diagnosen NAIT stilles ved at en påviser sirkulerende blodplatespesifikke antistoffer hos mor som reagerer med blodplateantiger uttrykt på barnets blodplater og som mor selv mangler. Flere studier viser at NAIT er underdiagnostisert i dagens praksis (8-10).
Gravide kvinner undersøkes ikke rutinemessig for blodplateantistoff. Dersom en kvinne tidligere har født et barn med alvorlig NAIT, er det ulik praksis for hvordan neste svangerskap følges opp. Intrauterin føtal blodprøvetaking og transfusjon til foster er en effektiv behandling for NAIT, men en slik behandling er risikofylt og faren for komplikasjoner hos fosteret er betydelig med 5,3 prosent risiko for fosterdød per prosedyre (11). En annen type behandling er å gi den gravide store doser (1g/kg/uke) intravenøst immunglobulin (IVIg), eventuelt med tillegg av steroider, for å redusere faren for alvorlig NAIT og NAIT-relaterte komplikasjoner. Effekten av behandling med IVIg er noe usikker. Flere studier viser effekt ved maternell IVIg behandling (12-15), og da særdeles ved mindre alvorlig NAIT (16,17), mens andre studier ikke finner samme effekt (18-21). I Norge er det i dag anbefalt at kvinner i påfølgende svangerskap med risiko for å føde et barn med alvorlig NAIT, følges opp med ultralydundersøkelser for å avdekke eventuelle blødninger, og at barnet forløses med keisersnitt noen uker før termin for rask behandling med transfusjon av forlikelige blodplater.
Denne oversiktsartikkelen bygger i hovedsak på resultater fra et kombinert screening- og intervensjonsprogram som ble gjennomført i store deler av Norge i perioden desember 1995 til mars 2004(3; 22-24). Studien startet ved UNN etter initiativ fra avdeling for immunologi og transfusjonsmedisin som har referanselaboratorium innen avansert blodplate immunologi, i samarbeid med kvinneklinikken og barneavdelingen ved UNN. Studien ble senere utvidet (september 2001) til et samarbeidsprosjekt mellom UNN, Ullevål universitetssykehus og Rikshospitalet. Ideen var at identifikasjon av risikograviditeter og enkel klinisk intervensjon ville kunne gi helsegevinst. Strategien var tredelt; 1) redusere tiden barnet ble utsatt for skadelige anti-HPA 1a antistoffer, 2) skånsom forløsning for å forhindre mulige traumer mot barnets hode og 3) tilrettelegge for umiddelbar behandling av nyfødte med alvorlig NAIT. Resultatet av screeningen (antall nyfødte med NAIT-indusert hjerneblødning eller intrauterine dødsfall) ble sammenlignet med resultater fra andre publiserte studier identifisert etter litteratursøk utført på PubMed (3). Kostnader i forbindelse med innføring av et screening- og intervensjonsprogram ble kalkulert og sammenlignet med antatte reduserte utgifter på grunn av unngått NAIT-relatert hjerneskade (7, 23). Videre benyttes relevante artikler fra eget litteraturarkiv innen fagområdet.
Effekt ved screening
I den norske screening- og intervensjonsstudien (3) ble alle gravide som var inkludert, typet for HPA 1a i samme blodprøve som var sendt for RhD typing. Blodprøver fra de gravide som var HPA 1a negative, ble analysert for å påvise en eventuell immunisering. Immuniserte HPA 1a negative (HPA 1bb) kvinner ble fra svangerskapsuke 30 fulgt opp med ultralydundersøkelse for å påvise eventuelle blødninger hos fosteret som ville kreve rask intervenering. Samtlige kvinner ble forløst med keisersnitt to til fire uker før termin, og nyfødte med alvorlig NAIT ble umiddelbart behandlet med forlikelige blodplater.
Resultatet av screening- og intervensjonsprogrammet viste at ca 32 prosent av de immuniserte kvinnene fødte barn med alvorlig NAIT (3). To barn fikk påvist hjerneblødning og en av disse utviklet alvorlige nevrologiske sekveler. I tillegg var det et intrauterint dødsfall hos en kvinne som primært var identifisert som HPA 1bb, men som ikke var fulgt opp videre i programmet. Resultatene fra screening- og intervensjonsprogrammet ble sammenlignet med andre relevante, publiserte studier. Sammenligningene viste at det norske screening- og intervensjonsprogrammet hadde 73 prosent færre NAIT-relaterte komplikasjoner knyttet til alvorlig NAIT (RR=0,27, 95 % CI: 0,08-0,92; p= 0,034).
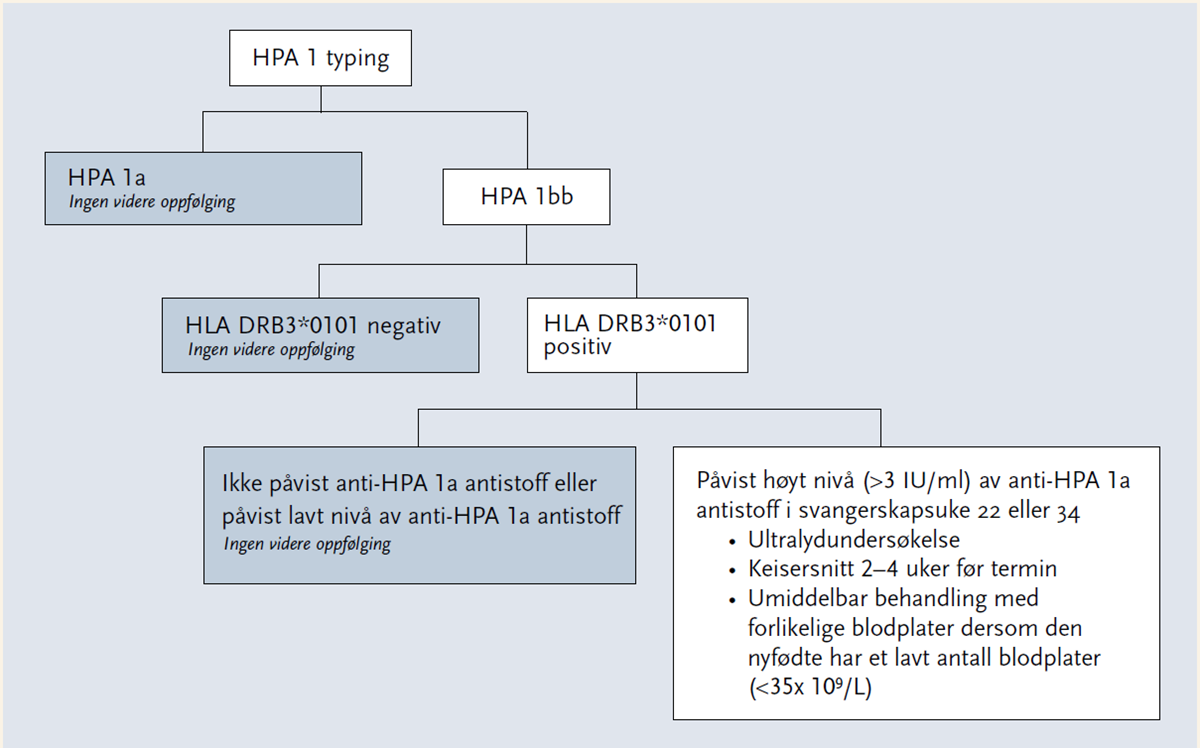
Videre viste studien at de fleste som ble immunisert var HLA DRB3*0101 positiv (3), og at alvorlighetsgraden av NAIT var relatert til mengde anti-HPA 1a antistoff i mors sirkulasjon (22, 24). Dette betyr at ved å selektere ut HPA 1a negative, HLA DRB3*0101 positive kvinner med høyt anti-HPA 1a antistoffnivå, kan en identifisere en gruppe kvinner som har høy risiko for å føde barn med alvorlig NAIT. Et flowdiagram som illustrerer et slikt screeningsprogram er vist i figur 1. HLA DRB3*0101 negative kvinner og kvinner med konstant lavt nivå av anti-HPA 1a antistoff, hadde svært lav risiko for å føde barn med alvorlig NAIT.
Kostnader ved screening
Et screening- og intervensjonsprogram ble kalkulert til årlig å koste ca 4 millioner kroner, eller ca 65 kroner per svangerskap (23). Helsekostnadene ved innføring av et kombinert screening- og intervensjonsprogram ble sammenlignet med antatte helsebesparelser som konsekvens av at færre barn fødes med nevrologiske sekveler på grunn av færre NAIT-relaterte komplikasjoner. Gjennomsnittlig livslang medisinsk kostnad for en person med cerebral parese (CP) ble i en amerikansk studie beregnet til 2,9 millioner kroner (25). Kostnader for NAIT-induserte nevrologiske sekveler ble satt til samme kostnad som for CP. Målet med den økonomiske analysen var å estimere forventede helsekostnader per vunnede kvalitetsjusterte leveår (Quality adjusted life years = QALYs) ved innføring av et nasjonalt screening- og intervensjonsprogram.
I Norge vil det årlig være ca 1200 gravide som er HPA 1a negative, og ca 120 gravide vil få påvist anti-HPA1a antistoff. Videre vil ca 38 barn fødes med alvorlig NAIT, og uten klinisk intervensjon kombinert med rask behandling kan en forvente 7,5 nyfødte med alvorlige NAIT-relaterte komplikasjoner (3).
Den økonomiske analysen viste at innføring av et effektivt screening- og intervensjonsprogram årlig, vil øke antall QALYs samtidig som statens helseutgifter reduseres (base case estimater) (23). Usikkerhetene i analysen ble kartlagt ved hjelp av en sensitivitetsanalyse og viste at et kombinert screening- og intervensjonsprogram var kostnadseffektiv også ved svært konservative effektestimater (23).
Diskusjon
Gjennomføringen av en randomisert screening- og intervensjonstudie ble nøye vurdert ved oppstart av den norske screeningsstudien, men det ble vurdert som etisk uforsvarlig å randomisere en gruppe immuniserte gravide kvinner til ingen oppfølging/beredskap i forbindelse med og like etter fødselen (3). Resultatet av studien ble istedenfor sammenlignet med historiske kontroller, og det er derfor viktig å være oppmerksom på begrensingene ved å sammenligne effekt av en intervensjon og/eller en behandling med resultater fra tidligere publiserte studier. Faren for bias er alltid til stede ved gjennomføring av en ikke-randomisert studie. Dette tatt i betraktning, gir studien likevel lovende resultater og det tyder på at en screening som inkluderer et intervensjons/behandlingsprogram, reduserer komplikasjoner hos nyfødte med alvorlig NAIT.
Årsaken til at intervensjons- og behandlingsprogrammet hadde effekt i form av et redusert antall NAIT-relaterte komplikasjoner, kan skyldes en kombinasjon av flere tiltak:
- Ved å avslutte svangerskapet før termin, kutter en ned risikoperioden for intrauterine komplikasjoner.
- Et skånsomt keisersnitt kan være mindre traumatisk for et barn med alvorlig trombocytopeni enn en vaginal forløsning, spesielt dersom den vaginale fødselen blir langvarig og komplisert. Selv om dette ikke er bevist i en randomisert studie, er keisersnitt anbefalt hos gravide kvinner med ideopatisk trombocytopenisk purpura (ITP) dersom platetallet hos barnet er lavt (26). Videre er det påvist at usymptomatiske hjerneblødninger normalt forekommer ved vaginale fødsler (27), men ikke ved keisersnitt.
- Umiddelbar behandling av nyfødte med alvorlig NAIT reduserer faren for komplikasjoner etter fødselen.
Et blodplatetall hos foster/nyfødt på < 20x109/L er forbundet med stor blødningsfare (28). I den norske studien var det to nyfødte med hjerneblødning (3). Disse hadde et blodplatetall på henholdsvis 26x109/L og 13x109/L. Det mangler lokale data på alvorlighetsgraden og langtidsvirkningene etter alvorlige blødninger hos foster/nyfødt med alvorlig NAIT, men internasjonale studier har vist at NAIT-relatert hjerneblødning hos foster eller nyfødt gir en betydelig risiko for alvorlig hjerneskade eller død. En større engelsk studie rapporterte alvorlig hjerneskade hos 80 prosent av nyfødte med NAIT-indusert hjerneblødning (4). Likeledes har en kanadisk studie vist at hos nyfødte diagnostisert med hjerneblødning, var 20 prosent forårsaket av trombocytopeni på grunn av antistoff mot HPA 1a. Samtlige av disse barna hadde alvorlig hjerneskade (29). I den norske studien hadde 16 nyfødte et blodplatetall lavere enn 10x109/L og hadde dermed betydelig fare for alvorlige blødninger. Det er stor sannsynligheten for at den raske behandlingen med kompatible blodplater forhindret alvorlige blødning etter forløsning hos disse.
Tidspunktet for når hjerneblødning kan oppstå er noe usikkert. To litteraturstudier rapporterte hjerneblødning intrauterint (som oftest mot slutten av svangerskapet) i 45 og 80 prosent av tilfellene (7, 30). To større retrospektive studier rapporterte hjerneblødning som oftest i forbindelse med eller etter fødselen (4, 6). I den norske studien ble det påvist én hjerneblødning intrauterint (svangerskapsuke 34) og én hjerneblødning etter forløsning (3).
Kost-nytte analysen viser at ved et effektivt behandlingsprogram for NAIT, er det mulig å etablere en screening som er kostnadseffektiv (23). Kostandseffektiviteten kan forklares ved at det er tilgjengelig enkle og rimelige metoder for å HPA 1 type i samme blodprøve som sendes til laboratoriet for Rh-D typing (31). Forløsning ved hjelp av keisersnitt og transfusjon til den nyfødte med alvorlig NAIT er også en forholdsvis enkel og rimelig behandling for å forhindre blødning som kan føre til en alvorlig funksjonshemming. Videre kan man velge enten å følge opp alle HPA 1bb gravide med anti-HPA 1a antistoff og dermed identifisere alle nyfødte med NAIT. Ulempen er imidlertid at det med en slik strategi utføres unødvendige keisersnitt der barnet viser seg å ha normalt blodplatetall. Alternativt kan man kan velge å identifisere en høyrisikogruppe og tilby oppfølging og intervensjon kun til disse. Dersom man velger å tilby oppfølging kun til en høyrisikogruppe, vil fem prosent av barn med alvorlig NAIT ikke få tilbud om rask behandling (32).
Konklusjon
Den norske studien viser at et kombinert screening- og intervensjonsprogram synes å redusere sykdom og død relatert til NAIT til om lag en fjerdedel. Videre viser studien at et effektivt screening- og intervensjonsprogrammet er kostnadsvarende. Resultatet fra studien ble presentert for Helse og Sosialdirektoratet høsten 2007 og et nasjonalt screening- og intervensjonsprogram vurderes nå av de sentrale helsemyndigheter.